Алюминий и химикаты
Благодаря защитным свойствам естественного оксидного слоя, алюминий проявляет хорошую стойкость ко многим химикатам. Однако, в среде с низким или высоким рН (менее 4 и более 9) происходит растворение оксидного слоя и, следовательно, ускоренная коррозия алюминия. Поэтому неорганические кислоты и концентрированные щелочные растворы являются для алюминия очень коррозивными.
Исключениями из выше упомянутого являются концентрированная азотная кислота и растворы аммиака. Они не вызывают коррозии алюминия.
В умеренных щелочных водных растворах коррозию можно замедлить путем применения силикатов в качестве ингибиторов. Такие ингибиторы включают в моющие растворы.
Большинство неорганических солей не являются особенно коррозивными для алюминия. Соли тяжелых металлов составляют здесь исключение. В результате реакции восстановления тяжелых металлов на поверхности алюминия она может подвергаться серьезной гальванической коррозии. Примером такого тяжелого металла служит медь.
Алюминий имеет хорошую стойкость к многим органическим соединениям. Алюминиевое оборудование применяют в производстве и хранении многих органических химикатов.
Алюминий в контакте с бетоном
Применение алюминия в строительной отрасли заставляет его вступать в контакт с большинством материалов, которые применяются в строительстве: бетоном, гипсом, полимерами и т. п.
Воздействие бетона
Алюминий хорошо противостоит воздействию бетона и цементного раствора, не смотря на их высокие щелочные свойства с величиной pH около 12. Когда бетон начинает схватываться, всегда происходит незначительное протравливание алюминия глубиной не более 30 мкм. Это воздействие, однако, замедляется через несколько дней контакта (рисунок 6). Это приводит к очень локализованному снижению величины pH до 8 единиц и образованию на поверхности алюминия защитной пленки из алюмината кальция.
Аналогично бетон воздействует на алюминиевые литые детали. Это повышает адгезию между этими материалами. После того, как бетон затвердеет (высохнет), коррозии обычно уже не происходит. Однако там, где влага накапливается и сохраняется, может развиваться коррозия. Увеличенный объем продуктов коррозии может вызвать в бетоне образование трещин.
Защита алюминия от воздействия бетона
Поэтому брызги влажных щелочных строительных материалов, например, раствора и бетона, оставляют поверхностные, но хорошо видимые пятна на алюминиевых поверхностях. Поскольку эти пятна трудно удалить, то видимые алюминиевые поверхности должны быть защищены, например, на строительных площадках.
Этот тип коррозии можно эффективно предотвратить путем окраски алюминия битумом или красками, стойкими в щелочной среде. Поскольку оксидное покрытие разрушается в сильно щелочной среде, то анодирование алюминия в этом случае не годится в качестве защиты от коррозии.
Считается, что в сухой атмосфере внутри здания в контакте с полностью затвердевшим бетоном алюминий не требует никакой коррозионной защиты.
Влияние хлоридов
В бетон обычно добавляют до 3 % хлорида кальция, чтобы ускорить схватывание бетона, а также предотвратить его замерзание в зимнее время. Это приводит к существенному снижению удельного электрического сопротивления бетона, а также его способности удерживать влагу. Все это способствует повышению коррозионной активности бетона.
Алюминий в пресной воде
Физическая химия воды
Вода является сильным растворителем, который способен растворять:
- многие неорганические и органические соединения,
- жидкости, если они являются полярными и содержат гидроксильную группу;
- газы.
- неорганических солей;
- растворенных газов;
- твердых веществ в виде суспензии и
- органических веществ.
Однако не все эти растворенные элементы влияют на коррозию алюминия. Основное влияние на коррозию алюминия оказывают растворенные в воде :
- хлориды;
- ионы тяжелых металлов.
Влияние концентрации хлоридов
Обще признано, что среди всех анионов хлоридные ионы имеют самую высокую способность проникать в естественную оксидную пленку на поверхности алюминия . Это происходит потому, что эти ионы очень маленькие и очень мобильные. Известно, что хлориды, а также фториды, бромиды и иодиды относятся к анионам, которые активируют коррозию алюминия в воде (рисунок 4), тогда как сульфаты, нитраты и фосфаты меньше активируют такую коррозию (рисунок 5.1) или вообще ее не активируют. Особенность хлоридов заключается в том, что они могут заменять атомы кислорода в оксидной пленке алюминия. Это приводит к ослаблению стойкости оксидной пленки к коррозии .
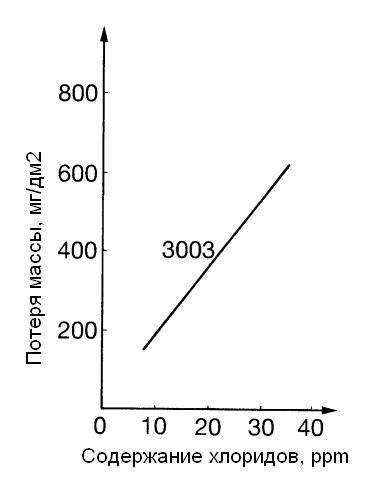
Рисунок 4 – Влияние концентрации хлоридов на стойкость к коррозии сплава 3003 в пресной воде
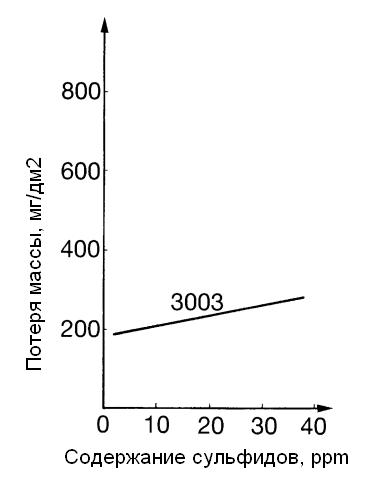
Рисунок 5.1 – Влияние концентрации сульфатов на стойкость к коррозии сплава 3003 в пресной воде
Точечная коррозия
В естественной пресной воде и водопроводной воде алюминий может подвергаться язвенной (точечной) коррозии (рисунок 5.2). Однако, при регулярной чистке и сушке риск серьезной коррозии очень мал. Алюминиевые кастрюли, котелки и сковородки, а также солдатские алюминиевые миски, ложки и кружки служили верой – правдой десятилетиями без каких-либо признаков коррозии.
Вероятность коррозии повышается, если вода стоячая, а алюминий находится влажным в течение длительных периодов.
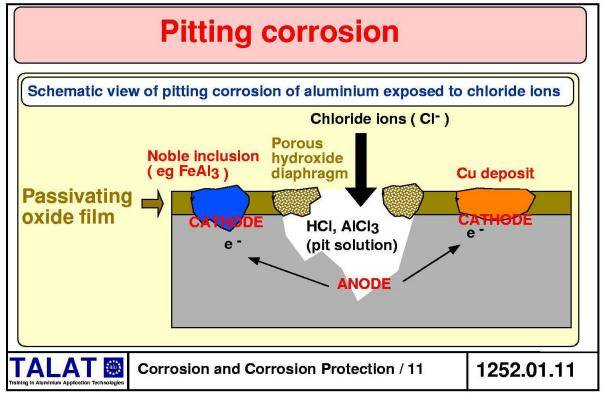
Рисунок 5.2 – Точечная коррозия алюминия
Влияние меди
Присутствие в алюминиевых сплавах меди значительно снижает их коррозионную стойкость. Такие сплавы применяют только при условии их надежной коррозионной защиты.
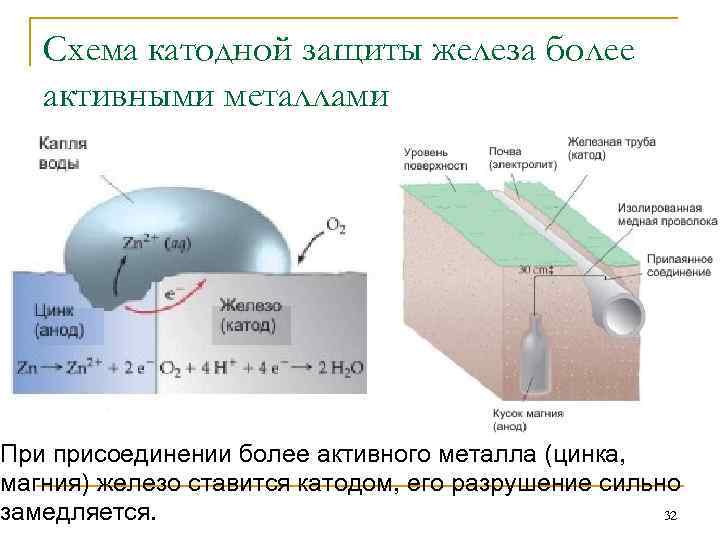
Принцип батареи
Гальваническая коррозия работает как батарея, которая состоит из двух электродов:
- катода, где происходит реакция восстановления
- анода, где происходит реакция окисления.
Эти два электрода погружены в проводящую жидкость, которая называется электролитом. Электролит – это обычно разбавленный кислотный раствор, например, серной кислоты, или соляной раствор, например, сульфат меди. Эти два электрода соединены снаружи электрической цепью, которая обеспечивает циркуляцию электронов. Внутри жидкости передача электрического тока происходит путем перемещения ионов. Жидкость, таким образом, обеспечивает ионное электрическое соединение (рисунок 9).
Рисунок 9 – Принцип гальванической ячейки
Рисунок 1 показывает ячейку, в которой электролитом является раствор серной кислоты. Серная кислота полностью диссоциирована в воде (поскольку является сильной кислотой) путем образования ионов Н+, которые определяют кислотность среды. Происходит следующая электрохимическая реакция :
цинковый анод окисляется:
Zn → Zn2+ + 2e−
на медном катоде восстанавливаются протоны Н+:
2Н+ + 2e− → Н2
Полная реакция имеет вид:
Zn + H2O → Zn(OH)2 + H2
Эта ячейка производит электричество за счет потребления цинка, который выделяется в виде гидроксида цинка Zn(OH)2.
Для работы ячейки необходимо одновременное выполнение трех условий:
- два различных металла, которые образуют два электрода;
- присутствие электролита;
- непрерывность всей электрической цепочки.
Если хотя бы одно из этих условий не выполняется, например, если нарушается электрический контакт, то ячейка не будет производить электричество, и окисления на аноде не будет происходить (также как и восстановления на катоде).
Способы борьбы с коррозией алюминия

Алюминий – широко распространенный в промышленности и быту металл. Окисление алюминия на воздухе не происходит. Его инертность обусловлена тонкой оксидной пленкой, защищающей его. Однако под влиянием определенных факторов из окружающей среды этот метал все же подвергается разрушительным процессам, и коррозия алюминия — не такое уж и редкое явление.
Механическое покрытие
Как защитить алюминий от коррозии? Чаще всего применяют механический способ – нанесение слоя краски.
Покройте краской изделие и вы убедитесь в действенности этого способа. Окрашивание бывает мокрым и сухим, или порошковым. Эти технологии усовершенствуются. При мокром окрашивании лакокрасочные слои наносят после защиты алюминия составом, содержащим соединения цинка и стронция. Металлическую основу тщательно подготавливают: защищают, шлифуют, сушат. Грунт наносят поэтапно.
Когда растворитель из грунтовочной смеси полностью исчезнет, поверхность можно покрывать изолирующим составом: масляным или глифталиевым лаком.
Специальные составы помогают остановить коррозию и защищают алюминиевые конструкции от химикатов, бензина, различного вида масел. Выбор покрытия зависит от условий последующей эксплуатации металлического изделия:
- молотковые – применяют для получения конструкций различных цветовых оттенков, используемых в декоре;
- бакелитовые – наносят под высоким давлением, заполняя микротрещины и поры.
Порошковое окрашивание требует тщательной очистки поверхности от жира и различных отложений. Это достигается погружением в щелочные или кислотные растворы с добавлением смачивателей. Далее на алюминиевые конструкции наносится слой хроматных, фосфатных, циркониевых или титановых соединений. После этого он не будет окисляться.
После просушки материала на окислившийся участок наносят защитный полимер. Чаще всего используются полиэфиры, стойкие к механическому, химическому и термическому воздействию. Применяют полимеризованный уретан, эпоксидные и акриловые порошки.
Оксидирование алюминия
Оксидирование алюминия протекает при постоянном токе под напряжением 250 В. Наращивание защитной пленки происходит при комнатной температуре с водяным охлаждением. Не требуется импульсного источника. Пленки получаются плотными и прочными в течение 45-60 минут.
На плотность и цвет оксидного покрытия влияет температура электролита:
- пониженная температура образует плотную пленку яркого цвета;
- повышенная – формирует рыхлую пленку, требующую дальнейшей окраски.
Образовать защиту алюминия от коррозии можно электрохимической реакцией. Процесс разделен на несколько этапов:
1. На стадии подготовки алюминиевое изделие обезжиривают, погружая его в раствор щавелевой кислоты.
2. После промывания водой опускают в щелочной раствор, чтобы удалить неравномерно образовавшийся оксидный слой.
3. Для дополнительной окраски алюминиевые изделия погружают в соответствующие растворы солей. Чтобы заполнить образовавшиеся поры, металлический материал обрабатывают паром.
4. Затем изделие подвергают сушке. Анодное оксидирование может проводиться с применением переменного тока.
Для защиты от коррозии применяют химическое оксидирование – менее затратное, не требующее специального электрического оборудования и квалификации исполнителей. Используется несложный химический состав.
В процессе алюминирования полученная оксидная пленка толщиной в 3 мкм имеет салатный цвет, обладает высокими электроизоляционными свойствами, не пориста, не окрашивается.
Коррозия алюминия возникает вследствие находящихся рядом металлов, которые окислились. Предотвращению этот процесса способствует изоляция. Это могут быть прокладки из резины, битума, паронита. При покрытии ржавчиной применяются лак и другие изолирующие материалы. Других способов избавиться от этой проблемы пока нет.
Выбор средства
Если задачей стоит не просто избавление от почернений, но и сохранение блеска поверхности, то придётся внимательно отнестись к подбору вещества. Сплав такого рода является мягким, и его можно повредить простой жёсткой тряпкой. Мелкие царапинки испортят весь образ, и сделают плоскость матовой. Однако можно исправить ситуацию, если приобрести обычное средство для полировки. Например, паста ГОИ прекрасно справиться с этой проблемой. Что относиться к безопасному устранению изъянов, то отдавать предпочтение лучше щадящим методикам:
- мыльный раствор;
- пищевые кислоты;
- соли;
- канцелярский клей.
Мыльный раствор для удаления нагара
Препараты очищения для чистки алюминия можно отыскать и в магазине, но перед покупкой будет разумно ознакомиться с составом. Разумеется, промышленная химия стремительнее остальных справиться с поставленной задачей, но дальнейшее использование сковороды для приготовления пищи будет опасно.
Читать также: Тележка для ремонта автомобиля лежа своими руками
Другие типы коррозии
4.1. Коррозия под напряжением
Коррозия под напряжением, которая ведет к образованию трещин, является более редким типом коррозии. Этот тип коррозии случается в основном в высокопрочных сплавах, таких как сплавы серий 2000 (AlCu) и 7000 (AlZn), а также серии 5000 (AlMg) при содержании магния более 4 %. Это происходит, когда металл подвергается длительным растягивающим напряжениям в присутствии коррозионной среды. Этот тип коррозии обычно не возникает в алюминиевых сплавах AlMgSi серии 6000, в том числе, в популярных сплавах 6060 и 6063 .
4.2. Межкристаллитная коррозия
Межкристаллитной коррозии подвергаются границы зерен металла, а не сами зерна. Сплавы серии 6000, например, 6060 и 6063, обычно являются стойкими к межкристаллитной коррозии. Образование в профилях рекристаллизованной структуры (с большим размером зерен), а также высокое содержание кремния и меди может способствовать коррозии такого вида. Для предотвращения или минимизации рекристаллизации в алюминиевые сплавы добавляют марганец и хром.
Межкристаллитная коррозия особенно характерна для сплавов серии 7000. Здесь она связана с выделениями MgZn, которые являются очень анодными по сравнению с алюминием и поэтому подвергаются коррозии .
4.3. Подповерхностная коррозия
Подповерхностная коррозия является видом выборочной коррозии, которая распространяется под поверхностью металла по одной или нескольким плоскостям. Этот вид коррозии возникает в основном в прокатных изделиях из высокопрочных сплавов серий 2000, 5000 и 7000.
Анодирование алюминия в сернокислом электролите.
Стандартный потенциал алюминия -1,67 В, но вследствие его склонности к пассивации он приобретает меньший отрицательный потенциал (-0,5 В). Коррозионная стойкость алюминия и его сплавов зависит от количества примесей или специально введенных в них добавок, а также от качества и вида окисного покрытия.
Процесс получения эмаль-покрытий находит все более широкое применение для защиты от коррозии, защитно-декоративной отделки или придания алюминию и его сплавам специальных свойств (электроизоляция, светопогло-щение и др.).
Анодирование в сернокислом электролите. Детали, изготовленные из Д16, AMг1, ABT-1 и других сплавов методом штамповки или точения, а также методом литья из сплавов АЛ9, АЛ11, АЛ22, АЛ32 с целью повышения коррозионной стойкости и улучшения товарного вида, анодируют в растворах серной кислоты. Подготовка деталей под анодирование в основном ведется по технологии, применяемой в гальванотехнике при покрытии изделий из алюминия и его сплавов.
Сернокислый электролит анодирования содержит 170-250 г/л H2SO4 (1,8-1,82). Режим анодирования: температура электролита 13-26°С; iа = 0,5- — 1,5 А/дм2; напряжение 10 — 25 В; Sа:Sк изменяется от 1:1 до 1:5; катод — из свинца; Sa = 0,5 ÷ 1,0 дм2/л, время анодирования 30 — 50 мин. В процессе анодирования по мере роста окисного покрытия плотность тока самопроизвольно падает. После соответствующей промывки в холодной, а затем в горячей воде, детали загружают в ванну с целью гидратирования окисла и замыкания пор в результате увеличения объема окисла. Раствор состоит из К2Cr2O7 (100 г/л) и Na2CO3 (18 г/л). Температура раствора 90 — 95°С, рН = 6 ÷ 7, продолжительность наполнения до 10 мин. Далее детали промывают в сборнике для улавливания хромпика в горячей воде и сушат в специальных камерах, обогреваемых калорифером или теплоэлектронагревателями с принудительной циркуляцией горячего воздуха. Окисное покрытие можно гидратировать в горячей воде без добавок наполнителя.
С увеличением концентрации серной кислоты пленка растет медленнее, так как более концентрированный раствор быстрее растворяет растущую пленку. Такие пленки отличаются большей пористостью и лучше заполняются хроматом или красителем.
После включения тока за 1-2 мин напряжение достигает предельного значения, причем с увеличением силы тока напряжение увеличивается незначительно. Это указывает на то, что при более высоких значениях iа получаются пленки с меньшим сопротивлением вследствие нагревания электролита, находящегося в порах. Поэтому в процессе анодирования необходимо постоянное охлаждение электролита. Оптимальную плотность тока надо выбирать с учетом температуры (рис. 132).
Рис. 132. Зависимость между напряжением и плотностью тока при сернокислом анодировании чистого алюминия
При повышении температуры электролита от 20 до 50°С толщина оксидной пленки уменьшается более чем в 10 раз.
Примеси хлоридов в электролите приводят к местным разрушениям пленки в результате концентрации тока и разъеданию металла в этих местах. Определенное влияние оказывает состав окисляемого металла (сплава). Дюралюминий и чистый алюминий анодируются легче, чем кремнистые сплавы. На силумине образуется более тонкая и менее пористая пленка, чем на чистом алюминии. Цвет пленки на силуминах темно-серый. Она не может быть окрашена в светлые тона. С увеличением содержания меди и кремния в сплавах получаются более тонкие и плотные пленки. В процессе анодирования концентрация серной кислоты в электролите естественно уменьшается, и ее добавляют согласно результатам химического анализа.
Окисные покрытия образованы в результате окисления основного металла и в отличие от металлических или Лакокрасочных покрытий обладают надежным сцеплением.
Твердость анодизационных покрытий на алюминии и его сплавах зависит от химического состава основного металла (сплава), а также от способа их нанесения. Наибольшую твердость имеют покрытия, получаемые на чистом алюминии в сернокислом электролите. Твердость окисных твердых покрытий близка к твердости естественного кварца и топаза (наждачная бумага не оставляет на них следов). Так, твердость окисного электроизоляционного покрытия, полученного из сернокислого электролита при 2,5 А/дм2, составляет 770 кгс/мм2 (при 14°С), а при 30°С и переменном токе 185-225 кгс/мм2.
Сплавы Mg-Al
Такие материалы широко используются в строительстве, пищевой и химической промышленности. Также их очень часто применяют в машиностроении. Считается, что неплохо подобные материалы подходят и для возведения сооружений, подвергающихся воздействию морской воды.
В том случае, если магния в состав сплава входит не более 3%, антикоррозийные свойства он будет иметь практически такие же, как и технический алюминий. Магний в таком сплаве находится в твердом растворе и в виде частиц Al8Mg5, равномерно распределенных по всей матрице.

Если этого металла в сплаве содержится больше 3%, частицы Al8Mg5 начинают выпадать по большей мере не внутри зерен, а по их границам. А это, в свою очередь, крайне негативно сказывается на антикоррозийных свойствах материала. То есть изделие становится гораздо менее устойчивым к ржавлению.
Что такое электрохимическая коррозия и может ли она быть на листе алюминия?
Вам будет интересно:Что такое «патриции»? Исторические сведения
Чаще всего появление электрохимической коррозии провоцируют гальванические пары. Повреждение появляется в месте соединения двух разных сплавов. В таком случае ржавчина будет явно бросаться в глаза. Важным моментом является то, что портится только один металл, а второй является источником запуска коррозионного процесса. Чтобы не бояться электрохимической коррозии, нужно использовать магниевый сплав. Специалисты из-за электрохимической ржавчины не рекомендуют использовать обычное железо при контакте с кузовом из алюминия.
Коррозия алюминия и его сплавов с цинком
Ржавеет Al, как уже упоминалось, медленнее, чем его сплавы. Касается это в том числе и материалов группы Al-Zn. Такие сплавы очень востребованы, к примеру, в самолетостроении. Некоторые их разновидности могут содержать медь, другие нет. При этом первый тип сплавов, конечно же, является к коррозии более устойчивым. В этом плане материалы Al-Zn сравнимы с магниево-алюминиевыми.
Сплавы этой разновидности с добавлением меди проявляют признаки некоторой неустойчивости к ржавлению. Но при этом разрушаются из-за коррозии они все же медленнее, чем изготовленные с использованием магния и Cu.

Оксидирование алюминия
Оксидирование алюминия протекает при постоянном токе под напряжением 250 В. Наращивание защитной пленки происходит при комнатной температуре с водяным охлаждением. Не требуется импульсного источника. Пленки получаются плотными и прочными в течение 45-60 минут.
На плотность и цвет оксидного покрытия влияет температура электролита:
- пониженная температура образует плотную пленку яркого цвета;
- повышенная – формирует рыхлую пленку, требующую дальнейшей окраски.
Образовать защиту алюминия от коррозии можно электрохимической реакцией. Процесс разделен на несколько этапов:
1. На стадии подготовки алюминиевое изделие обезжиривают, погружая его в раствор щавелевой кислоты.
2. После промывания водой опускают в щелочной раствор, чтобы удалить неравномерно образовавшийся оксидный слой.
3. Для дополнительной окраски алюминиевые изделия погружают в соответствующие растворы солей. Чтобы заполнить образовавшиеся поры, металлический материал обрабатывают паром.

4. Затем изделие подвергают сушке. Анодное оксидирование может проводиться с применением переменного тока.
Для защиты от коррозии применяют химическое оксидирование – менее затратное, не требующее специального электрического оборудования и квалификации исполнителей. Используется несложный химический состав.
В процессе алюминирования полученная оксидная пленка толщиной в 3 мкм имеет салатный цвет, обладает высокими электроизоляционными свойствами, не пориста, не окрашивается.
Коррозия алюминия возникает вследствие находящихся рядом металлов, которые окислились. Предотвращению этот процесса способствует изоляция. Это могут быть прокладки из резины, битума, паронита. При покрытии ржавчиной применяются лак и другие изолирующие материалы. Других способов избавиться от этой проблемы пока нет.
Неорганические соединения
Алюминий не стоек к действию кислот. Исключение составляют концентрированные азотная и серная кислоты — их окислительные свойства настолько сильны, что при контакте с алюминием на его поверхности образуется прочный слой оксида алюминия, препятствующий дальнейшему разрушению металла (поэтому концентрированную азотную или серную кислоту перевозят в алюминиевых цистернах). Разбавленная азотная или серная кислота — более слабый окислитель — энергично реагирует с алюминием.
В кислотах алюминий растворяется тем хуже, чем меньше содержит дополнительных примесей. Следует помнить, что анодное окисление не защищает от воздействия кислот, поскольку они разрушают слой Al2O3. Химическая активность кислот увеличивается с ростом температуры. Например, с возрастанием температуры на 10°С скорость коррозии удваивается. Увеличение концентрации кислоты, как правило, увеличивает скорость коррозии (концентрированные серная и азотная кислоты — исключение).
Соляная кислота вызывает сильную коррозию. Действие этой кислоты нельзя ослабить добавлением ингибиторов.
Фтороводородная кислота оказывает самое сильное влияние на алюминий. Даже непродолжительное взаимодействие разбавленной кислоты ведет к полному растворению алюминия.
Кислородсодержащие кислоты хлора (HClO4, HClO3, HClO) вызывают сильную коррозию алюминия.
Серная кислота вызывает равномерную коррозию алюминия, интенсивность которой зависит от концентрации. Разбавленная кислота средней концентрации при комнатной температуре отличается умеренной агрессивностью. Наиболее агрессивна кислота концентрации 80%. Некоторые вещества, входящие в состав алюминиевых сплавов, а также ионы, содержащиеся в воде (особенно фториды и хлориды), усиливают действие серной кислоты.
Сернистая кислота вызывает локальную коррозию алюминия.
Сера и халькогены (селен и теллур) на алюминий не действуют.
Фосфорная кислота разрушает алюминий умеренно или сильно (в зависимости от концентрации).
Мышьяк при комнатной температуре не действует на алюминий.
Мышьяковая кислота (H3AsO4) и окись мышьяка сильно разрушают алюминий, а мышьяковистая кислота (H3AsO3) без нагревания на него не влияет.
Азотистая кислота (HNO2) при комнатной температуре не действует на алюминий.
Азотная кислота (HNO3) воздействует на алюминий по-разному, в зависимости от концентрации. Разбавленные растворы интенсивно разрушают алюминий. В концентрированных растворах вследствие окислительных процессов поверхность алюминия пассивируется и коррозия замедляется. Наиболее сильную коррозию вызывает кислота концентрацией 10-60%. Действие азотной кислоты приводит к равномерной коррозии. С увеличением чистоты алюминия возрастает его стойкость к коррозии. Наличие в составе слава примесей меди, кремния, магния усиливает воздействие азотной кислоты.